728x90
반응형
안녕하세요 오늘은 지난 시간에 다뤘던 결합들에 대해 총 정리해보는 시간을 갖도록 하겠습니다.
고체 재료는 1차 결합과 2차 결합으로 구성되어있습니다.
1차 결합은 앞에서 다뤘던 금속, 이온, 공유결합이 이에 속하고,
2차 결합은 반 데르 발스 결합이 있습니다.
1차 결합은 최외각 전자들에 의해 이루어지며, 결합방식은 구성 원자들의 전자 구조에 의해서
정해지게 됩니다.
일반적으로 최외각 전자가 완전히 채워진 안정한 상태가 되기 위해 발생하는 현상이라고
볼 수 있습니다.
2차 결합은 물리적 결합이라고도 지칭하는데 이는 1차 결합에 비해 약하지만,
재료의 물성에 영향을 줍니다.
1. 금속결합
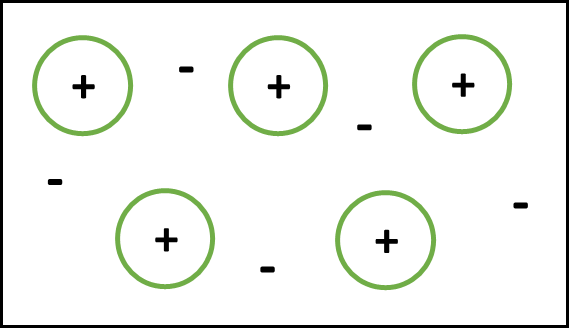
금속결합이란?
고체상에서 최외각 전자가 특정한 원자에 구속되어 있지 않고,
금속 내부를 자유롭게 돌아다니는 상태입니다.
자유전자는 양전하가 정전기적으로 서로 밀어내는 것을 막으며, 양전하를 서로 뭉치게 하는
역할을 합니다.
자유전자의 존재로 높은 전기&열전도도, 전성, 연성, 특유의 빛깔을 가집니다.
결합력의 경우에 '공유결합>이온결합>금속결합'으로 다른 고체 재료에 비해 결합력이 약합니다.
고체 재료 금속의 특징 (금속결합)
안녕하세요 오늘은 고체 재료 중에서도 금속의 특징에 대해서 좀 더 깊게 살펴보도록 하겠습니다. 고체 재료의 일반적인 특징은 각각 재료의 결합 형태 차이에 의해 설명이 가능합니다. 위는 그
yuljis.tistory.com
2. 이온결합
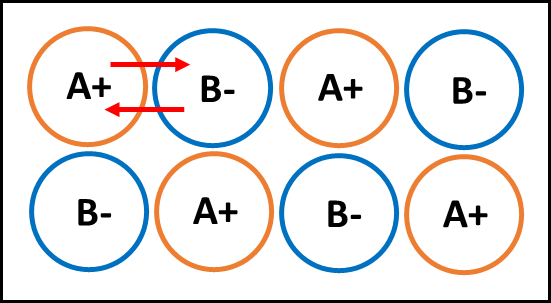
이온결합이란?
금속 원자와 비금속 원자가 만나 각각 전자를 잃거나 받아서 양이온과 음이온을 형성하며
안정된 전자 배치를 이룬 것을 말합니다.
이온결합은 양이온과 음이온, 두 이온 사이에 작용하는 정전기적 인력(쿨롱의 힘)에 의한 결합이며
쿨롱의 힘의 세기는 두 이온 간의 거리의 반비례하고 두 이온의 전하량의 비례합니다.

그렇기 때문에 이온간의 거리가 짧을수록, 두 이온의 전하량이 클수록
결합력이 증가하여 녹는점과 끓는점이 높아집니다.
이외에도 이온 결합의 특징은,
고체 상태의 경우 이온이 서로 결합하여 자유롭게 이동할 수 없어서 전기 전도성이 없고,
용융, 수용액 상태의 경우 이온들이 자유롭게 이동할 수 있어서 전기 전도성이 있습니다.
오늘은 1차 결합 중 금속결합, 이온결합 두 가지에 대해 알아봤습니다.
다음 시간엔 공유결합, 반 데르 발스 결합을 끝으로 마무리하겠습니다.
고체 재료의 결합 (공유결합, 반데르발스결합) (2)
안녕하세요? 오늘은 1차 결합의 공유결합과 2차 결합의 반데르발스결합에 대해서 설명드리고자 합니다. 3. 공유결합 공유결합 이란? 두 인접 원자 간에 최외각 전자를 공유하는 결합입니다. 공유
yuljis.tistory.com
반응형
'재료공학 > 재료 결합' 카테고리의 다른 글
| 고체 재료의 결합 (공유결합, 반데르발스결합) (2) (0) | 2022.11.21 |
|---|

댓글